Teknik för identifiering av unika enheter automatiserar avläsning av medicintekniska ID:n och streckkoder
Bidraget med av DigiKeys nordamerikanska redaktörer
2023-10-26
Under 2013 implementerade den amerikanska läkemedelsmyndigheten FDA regeln om Unique Device Identification System (system för identifiering av unik enhet). Regeln syftade till att förbättra patientsäkerheten genom att tillhandahålla en konsekvent metod för spårning och identifiering av medicintekniska produkter med hjälp av modern dokumentation vid tillverknings-, distributions- och användningspunkter. I likhet med kraven i de europeiska förordningarna om medicintekniska produkter eller liknande bestämmelser i andra länder, ökar den amerikanska UDI-regeln rapporteringsnoggrannheten och underlättar analys i händelse av ett återkallande eller en negativ händelse.
Från och med den 24 september 2023 kommer FDA att fullt ut tillämpa National Health Related Item Code och Drug Code Numbers på enheters etiketter och förpackningar. Alla medicinska produkter som märks på eller efter detta datum måste uppfylla UDI-kraven fullt ut. Denna bestämmelse kommer att ha inverkan på följande:
- Livskritiska produkter i klass 3 såsom pacemakers och implanterade proteser
- Måttligt viktiga produkter i klass 2 såsom sprutor, katetrar och absorberbara suturer
- Produkter med lägre risk i klass 1 såsom tandtråd, sjukvårdsrockar och syrgasmasker
Om en medicinteknisk produkt inte har en avläsbar streckkod kommer den inte längre att betraktas som en giltig/användbar produkt, även om den har etiketter som kan läsas av människor och även om produkten i allmänhet antas vara lätt att identifiera för de flesta användare. Denna fullständiga tillämpning kommer att leda till ett omfattande införande inom den medictekniska industrin och vid fakturering av sjukförsäkringar.
 Figur 1: Vissa handhållna DPM-streckkodsläsare (Direct Part Mark) har avancerad belysning och annan programvara som automatiskt hittar symboler och växlar mellan inställningar för att optimera avläsningen av det specifika DPM-märket och substratmaterialet i fråga. LVS-9585 som visas här kan verifiera både DPM-artiklar och tryckta etiketter för omfattande analys och rapportering. (Bildkälla: Omron Automation)
Figur 1: Vissa handhållna DPM-streckkodsläsare (Direct Part Mark) har avancerad belysning och annan programvara som automatiskt hittar symboler och växlar mellan inställningar för att optimera avläsningen av det specifika DPM-märket och substratmaterialet i fråga. LVS-9585 som visas här kan verifiera både DPM-artiklar och tryckta etiketter för omfattande analys och rapportering. (Bildkälla: Omron Automation)
Den upphandlande enheten (varumärkesinnehavaren) är ansvarig för
I USA är det ägaren av de immateriella rättigheterna och det användarorienterade varumärket för varje medicinsk produkt som ansvarar för att UDI-koderna är korrekta och av hög kvalitet. Detta är särskilt viktigt eftersom en så stor del av marknaden för medicinska produkter är kontraktstillverkad och utlokaliserad till andra organisationers anläggningar. Därför är det den upphandlande organisationens ansvar att se till att hela leveranskedjan är UDI-kompatibel och producerar korrekta etiketter.
Ursprunget till tekniken för identifiering av unika enheter (UDI)
UDI:er är statiska enhetsidentifierare. Ändringar av antalet artiklar i en förpackning kan dock leda till att en ny identifierare behövs. Utfärdande organ bestämmer hur dessa detaljer ska särskiljas. På samma sätt kan en ändring av sterilitetsvillkoren för en produkts förpackning också ändra produktens identifierare. Om en produkts destinationsmarknad (det land där produkten ska säljas), märkningsspråk eller CE-märkning ändras kan det också krävas ändringar av produktidentifieraren.
Före UDI-regeln kunde en tillverkare av medicinsk utrustning märka en produkt med ett visst artikelnummer. Distributören ändrade artikelnumret innan vårdgivaren eller sjukhuset skulle ändra det igen. Eftersom varje enhet kunde ändra artikelnumret innan det nådde patienten var det nästan omöjligt att spåra produkter, hantera återkallelser, förhindra förfalskningar eller beställa nya lager på ett effektivt sätt.
Relaterat: Implementering av robusta spårbarhetslösningar
För närvarande tilldelas varje enhet en standardiserad och beständig identifierare, en så kallad UDI, för att alla enheter ska kunna identifiera enheten snabbare och mer exakt, vilket i slutänden minskar antalet medicinska fel. Denna UDI är en alfanumerisk kod som innehåller två viktiga uppgifter:
- En enhetsidentifierare
- En produktionsidentifierare
En enhetsidentifierare är en statisk etikett som tilldelas en viss enhet och som anger etikettmärkaren (vanligtvis enhetstillverkaren) och enhetens specifika modellnummer. Däremot innehåller en produktionsidentifierare data som kan variera, och mycket av den data som den kan innehålla är valfri. Dessa kan omfatta koder för parti och batch, serienummer, utgångsdatum och tillverkningsdatum. Kort sagt kan de valfria uppgifterna vara vad som helst som en tillverkare eller etiketterare anser vara nödvändigt för att stödja spårning av enheter.
Varje UDI-märkning måste presentera denna information i två former:
- Läsbar form (vanlig text)
- Maskinläsbar form (läsbar av en streckkods- eller RFID-läsare)
När en produkt kan uppfylla flera medicintekniska tillämpningar måste UDI märkas direkt på produkten, inte på dess förpackning. Regeln gäller även för enheter som kan användas flera gånger.
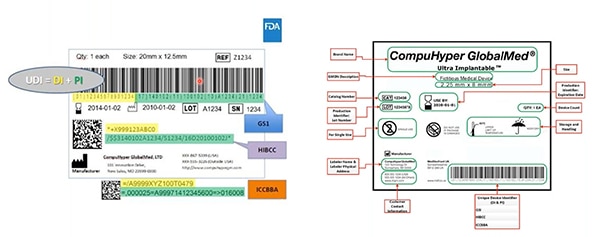 Figur 2: GS1, HIBCC och ICCBBA – UDI-utfärdande organ - skapar UDI:er, tilldelar UDI:er tillåten symbologi, definierar vilka tekniker som kan kopplas till UDI:er och specificerar den kvalitet som krävs för UDI-märkning. Enhetens identifierare är markerad med gult i detta prov. Produktionens identifierare är markerad med grönt. Andra element är information som kan läsas av människor ... och som också är kodad i den maskinläsbara streckkoden. (Bildkälla: FDA)
Figur 2: GS1, HIBCC och ICCBBA – UDI-utfärdande organ - skapar UDI:er, tilldelar UDI:er tillåten symbologi, definierar vilka tekniker som kan kopplas till UDI:er och specificerar den kvalitet som krävs för UDI-märkning. Enhetens identifierare är markerad med gult i detta prov. Produktionens identifierare är markerad med grönt. Andra element är information som kan läsas av människor ... och som också är kodad i den maskinläsbara streckkoden. (Bildkälla: FDA)
Alla produkter måste registreras i den globala UDI-databasen för att möjliggöra spårning i händelse av ett återkallande och för att ge allmänheten tillgång till information om en viss produkt. FDA-ackrediterade utfärdande organ är auktoriserade att skapa unika identifierare som tillverkare av enheter kan placera på sina produkter.
Relaterad vitbok: Håll dig uppdaterad om spårbarhet
Teknik och metoder för UDI-skanning
UDI-märkningar kan verifieras på flera sätt på deras väg från tillverkning till användning.
Inline-verifiering utförs av teknik som är integrerad i större maskiner för snabb och korrekt bearbetning av stora mängder produkter när de produceras. Dessa tekniker stöds av avancerad programvara och har ibland formen av etikettskrivare av industrikvalitet. Skrivarna kan utföra en egen inline-verifiering för att bekräfta att UDI-informationen är läsbar enligt stränga branschstandarder direkt när den skapas vid etikettproduktionen. Verifieraren V275 från Omron Automation är exempelvis avsedda att användas tillsammans med Zebras termotransferskrivare för att uppfylla standarderna ISO 15426 och GS1 för utfärdande organ, för FDA-överensstämmelse.
Relaterat: Omrons lösningar för spårbarhet
På andra håll sker inline-verifiering i form av specialiserad maskineseende vid sidan av transportband i automatiserade produktionslinjer, med streckkodsavläsning för extremt snabb och exakt verifiering av UDI-märkning på produkter med hög blandning i produktionslinjer med hög hastighet. MicroHAWK från Omron Automation utmärker sig inom detta område med avancerade sensorer som kompletteras av en miniatyrkonstruktion och anslutningsmöjligheter som inkluderar Ethernet/IP och PROFINET.
Relaterat: Undvik ansvaret för felaktig märkning
Däremot är offline UDI-verifiering bäst lämpad för batchprover av etiketter för att säkerställa kvaliteten. Offline-verifiering används ofta vid provning när medicintekniska produkter lämnar eller anländer till en anläggning, och kan komplettera onlineverifieringssystem tidigare i distributionskedjan.
 Figur 3: UDI:er som är direkt märkta på produkter kräver andra verifierare än de som används för UDI:er som är tryckta på fastsatta etiketter. (Bildkälla: Omron Automation)
Figur 3: UDI:er som är direkt märkta på produkter kräver andra verifierare än de som används för UDI:er som är tryckta på fastsatta etiketter. (Bildkälla: Omron Automation)
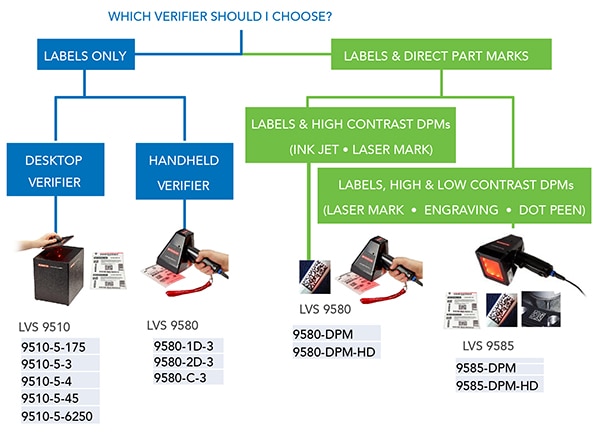
Faktum är att all medicinteknisk distribution och vårdverksamhet kan dra nytta av att använda ISO-kompatibla verifierare. Överväg Omrons serie LVS 95XX med offlineprodukter för UDI-verifiering. Dessa används:
- Vid lasermärkningsstationer och etikettskrivare där koder skapas
- När koder används på produkter, som kan vara separata från det område där koden skapas eller inte
- I kvalitetskontrollstationer där mallar, formatering och andra kodelement bekräftas
Specificering av offlinevariationer för UDI-verifierare
Vilken offline UDI-verifierare som är bäst lämpad för en viss tillämpning beror på flera parametrar.
Streckkodens storlek: Stora streckkoder är ofta lättare att skanna med identifierare som har ett stort synfält som definieras av objektivets brännvidd och sensorns storlek. Överväg den stationära UDI-identifieraren LVS-9510 från Omron Automation. Denna produktserie kan läsa både linjära etiketter och 2D-etiketter. Fem olika versioner har olika synfält så att konstruktörerna kan välja den version som är kompatibel med storleken på den streckkod som ska verifieras. En sammanflätningfunktion möjliggör gradering av streckkoder som överskrider synfältet.
Dessutom kan alla LVS-9510 automatiskt bestämma den symbologi och bländare som behövs för att utvärdera koden och identifiera och markera problemställen.
 Figur 4: Streckkodsverifiering som uppfyller ISO-standarderna underlättas med utrustning som kan verifiera både linjära (1D) och tvådimensionella (2D) koder. Viss sådan utrustning bestämmer den symbologi och bländare som behövs för att utvärdera koder samt identifierar och belyser problem. LVS-9510 som visas här har en sammanflätningsfunktion som möjliggör gradering av streckkoder som är större än synfältet. (Bildkälla: Omron Automation)
Figur 4: Streckkodsverifiering som uppfyller ISO-standarderna underlättas med utrustning som kan verifiera både linjära (1D) och tvådimensionella (2D) koder. Viss sådan utrustning bestämmer den symbologi och bländare som behövs för att utvärdera koder samt identifierar och belyser problem. LVS-9510 som visas här har en sammanflätningsfunktion som möjliggör gradering av streckkoder som är större än synfältet. (Bildkälla: Omron Automation)
Streckkodens typ: Skannrar måste läsa streckkodsformat som tilldelats av de utfärdande organen HIBCC, ICCBBA eller (vanligast från och med 2023) GS1. GS1 bestämmer storlek, format och upplösning för UPC, linjära streckkoder och 2D-streckkoder med datamatris.
UDI-märkningens placering: Överväg direkt delmärkning (DPM) av medicintekniska produkter. Dessa märkningar kan vara otroligt små, särskilt när de identifierar kirurgiska instrument och implanterbara medicintekniska produkter. Omrons handhållna verifieringsenheter LVS-9580 och LVS-9585 med ultrahög densitet har en speciallins som kan läsa av en mängd olika DPM:er, inklusive sådana med cellstorlekar ner till 0,002 tum. Linser av industrikvalitet i LVS-9580 och LVS-9585 garanterar konsekvent avläsningsnoggrannhet. Det mest sofistikerade är de mycket styrbara och kalibrerbara belysningsteknikerna inuti skannrarna. Tillsammans med flera synfält möjliggör belysningen omedelbar optimering av de tagna UDI-bilderna. Detta är särskilt viktigt eftersom kodstandarden inte tillåter några korrigeringar eller bildmanipulationer i efterhand.
Mer om programvara för UDI-skanning
För maximal effektivitet måste programvara för UDI med stöd för verifieringshårdvara presentera diagnostisk information i ett intuitivt format. Programvaran måste klassificera UDI-koder enligt ISO-definierade parametrar (viktigast är att bekräfta dess läsbarhet) och bör helst också spåra förvärrade problem över en serie av UDI-skanningar.
Omron inkluderar all nödvändig programvara med var och en av sina utrustningar för UDI-skanning. Programvaran uppdateras regelbundet för att hålla jämna steg med snabbt föränderliga regler och ny branschlagstiftning.
En viktig funktion i Omrons skannerprogramvara är hantering av kodsyntax. Kort sagt måste varje streckkod eller 2D-kod extrahera all relevant information korrekt, inklusive produkttyp, partinummer, kvantitet i förekommande fall, utgångsdatum, leveransinformation etc. De resulterande datasträngarna måste formateras på ett särskilt sätt för att hålla jämna steg med föränderliga krav, metoder och destinationer för medicintekniska produkter.
Regelbundet uppdaterad programvara från scannertillverkaren garanterar att slutanvändarna håller sig uppdaterade även när nya koder släpps.
Sammanfattning
Den amerikanska militären hade en gång som mål att fullt ut använda ett UID-produktspårningssystem liknande UDI-systemet inom den medicinska industrin. Syftet var att minska det enorma slöseriet med förlorade, duplicerade och oräknade leveranser vid militära anläggningar, inklusive allt från färdiga Raytheon-vapen till kontrollpaneler som levererats av ett litet företag för någon specialtillämpning. Idag används UID:er på olika sätt.
Samma öde kommer inte att drabba UDI-bestämmelsen.
Det mantra som driver införandet av UDI är okomplicerat: Etiketten är produkten. En felaktig etikett kan trots allt orsaka en kedja av händelser som slösar bort vårdpersonalens tid och leder till att den medicintekniska produkten kastas. Därför måste UDI:er finnas på alla lager av förpackningar, t.ex. på enhets-, förpacknings-, bunt-, låd- och pallnivå. UDI:er på sterila medicintekniska produkter innanför steriliseringsförseglingar är särskilt viktiga, eftersom det är oacceptabelt att bryta förseglingen för att verifiera enhetstypen.
Med FDA:s krav på fullständig efterlevnad av UDI-direktiven från och med den 24 september 2023 kommer avancerad skanningteknik för verifiering av medicinska produkter att bli avgörande för såväl automationstillverkare som de maskintillverkare och slutanvändare som de betjänar.
Sådana skannrar kan uppfylla mycket specifika UDI-krav från FDA för att bekräfta etiketter på ett stort utbud av utrustning för laboratorier samt medicinsk och klinisk diagnostik. Offline-streckkodsverifierare maximerar spårbarheten, inline-maskinseende och avancerade DPM-läsare.

Disclaimer: The opinions, beliefs, and viewpoints expressed by the various authors and/or forum participants on this website do not necessarily reflect the opinions, beliefs, and viewpoints of DigiKey or official policies of DigiKey.






